医疗器械注册是指根据国家法定程序,由食品药品监督管理部门对申请上市的医疗器械进行系统评价,以决定是否同意其上市销售的过程。对于二类医疗器械,这一过程尤为严格,需要企业投入大量的人力、物力和时间资源。根据《医疗器械监督管理条例》规定,第二类医疗器械是指具有中度风险、需要严格控制管理的医疗器械。作为医疗器械企业,掌握注册流程不仅是合规要求,更是产品顺利上市的关键。小编以广东省的二类医疗器械注册流程为例,讲述一下广东省二类医疗器械注册申报流程,帮助您能高效完成注册申报。
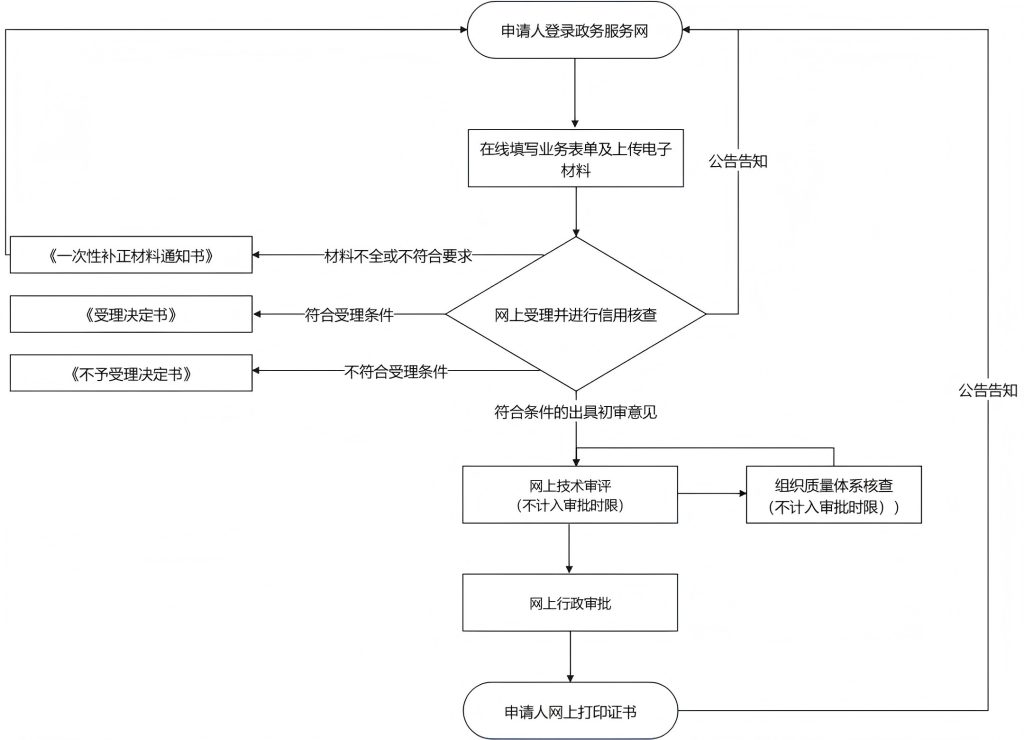
二类医疗器械办理流程步骤:
步骤1:收件
1. 申请事项依法不需要取得行政许可的,应当场告知申请人不予受理并出具不予受理通知书;
2. 申请事项依法不属于本行政机关职权范围的应当场出具不予受理通知书,并在受理通知书上告知申请人向相关行政机关提出申请;
3. 申请人隐瞒有关情况或者提供虚假材料申请的,出具不予受理通知书。
4. 不能当场审查不齐全或不符合法定形式的,当场出具收件通知书,五日内审查材料不齐全或不符合法定形式的,出具包含具体补正要求的一次性告知通知书;
5. 能当场判断申请材料需要补正的,应当场出具一次性告知通知书。
步骤2:受理
1. 能当场受理或通过当场补正达到受理条件的,直接进入受理步骤,当场出具受理通知书;
2. 根据一次性告知通知书内容进行补正后达到受理条件的,出具决定受理通知书;
3. 收件之日起5个工作日内未收到一次性告知通知书的,从收件之日起即为受理。
步骤3:审查
提出初步意见,转入决定步骤。
特殊程序:实地核查,专家评审,技术审查,其他/其他审查方式
受理之日起3个工作日内将申报资料转交技术审评机构。技术审评机构应当在40个工作日内完成第二类医疗器械注册的技术审评工作。如需补充资料,申请人应当在1年内按照补正通知的要求一次提供补充资料。企业补充资料后,技术审评机构应当自收到补充资料之日起30个工作日内完成技术审评。
步骤4:决定
1. 符合规定的,准予行政许可。
2. 不符合规定的,不准予行政许可。
办理时限为2个工作日。
步骤5:制证
准予行政许可决定书不准予行政许可决定书。
办理时限为5个工作日。
步骤6:送达
1. 准予行政许可的颁发《准予行政许可决定书》
2. 不予行政许可的颁发《不予行政许可决定书》
送达方式:主要以窗口领取、代理人送达、委托人送达、公告送达、邮寄送达,没有具体的办理时限。
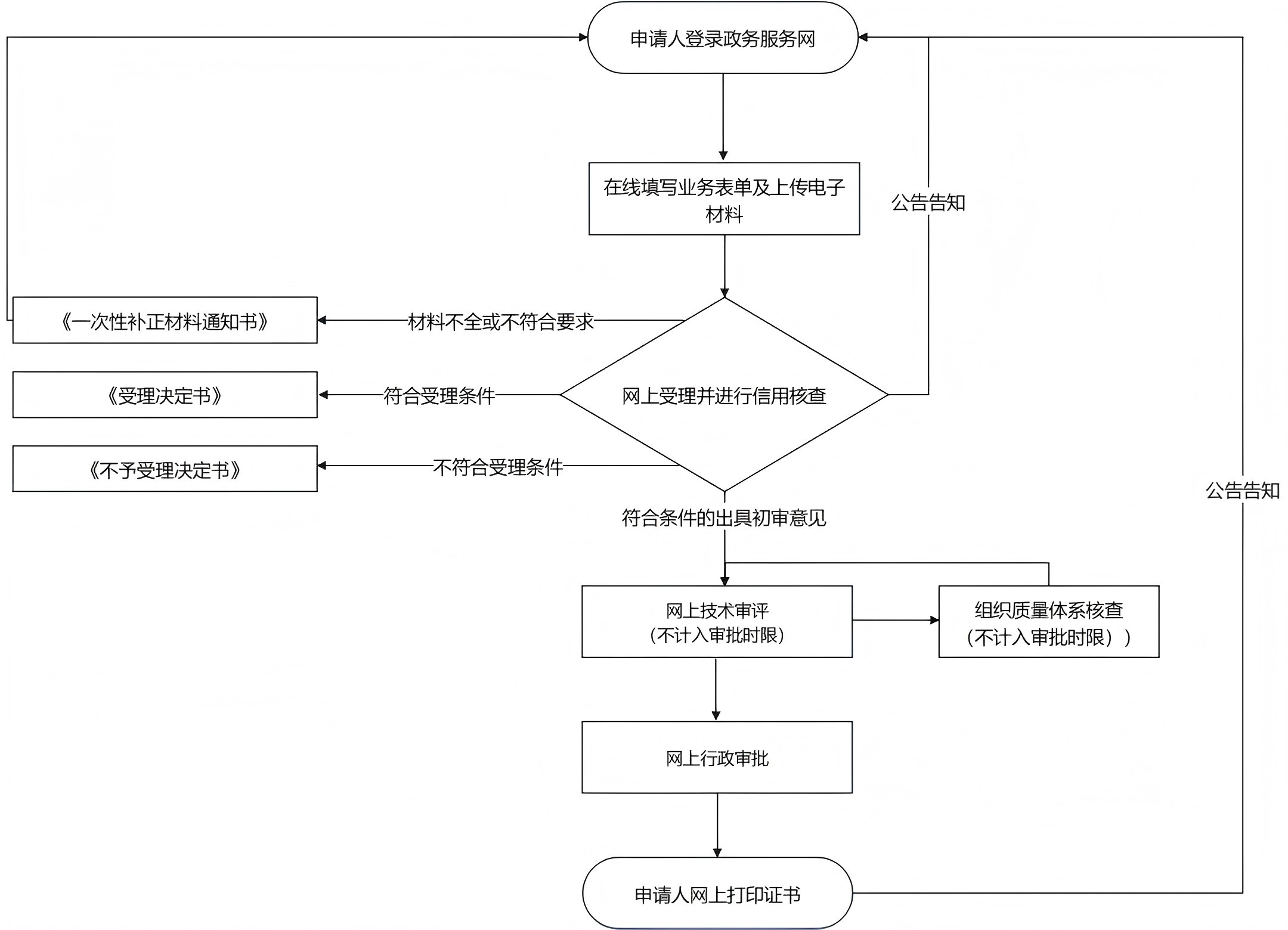
以下是我们公司二类器械注册的辅导流程的简图,供各位看官参考:
| 序号 | 材料名称 | 材料要求 |
| 1. | 医疗器械注册申请表 | 从广东省药品监督管理局网站(WWW.GDDA.GOV.CN)下载并根据要求填写。 |
| 2. | 监管信息 | 1. 章节目录2. 申请表3. 术语、缩写词列表4. 产品列表5. 关联文件6. 申报前与监管机构的联系情况和沟通记录7. 符合性声明 |
| 3. | 综述资料 | 1. 章节目录2. 概述3. 产品描述4. 适用范围和禁忌证5. 申报产品上市历史6. 其他需说明的内容 |
| 4. | 非临床资料 | 1. 章节目录2. 产品风险管理资料3. 医疗器械安全和性能基本原则清单4. 产品技术要求及检验报告5. 研究资料6. 非临床文献7. 稳定性研究8. 其他资料 |
| 5. | 临床评价资料 | 1. 章节目录2. 临床评价资料3. 其他资料 |
| 6. | 产品说明书和标签样稿 | 1. 章节目录2. 产品说明书3. 标签样稿4. 其他资料 |
| 7. | 质量管理体系文件 | 1. 质量管理体系文件a. 综述b. 章节目录c. 生产制造信息d. 质量管理体系程序e. 管理职责程序f. 资源管理程序g. 产品实现程序h. 质量管理体系的测量、分析和改进程序i. 其他质量体系程序信息j. 质量管理体系核查文件2. 注册申请人基本情况表 |
| 8. | 营业执照 | 营业执照复印件 |
注意:营业执照关联电子证照可免提交
参考网址:https://www.gdzwfw.gov.cn/portal/v3/guide/11440000MB2D0344212440172015007
第二类医疗器械注册证核发
下次咱们分享一下二类注册证资料清单的具体要求。



于2025年12月17日发布的《医疗器械注册手册》-300x191.png)
